Introduction
これまでの常識:
「造血幹細胞=HSC」という1つの祖先から(中間血球を経て)様々な血球に分化する。
※中間血球:「骨髄球系血球にのみ分化できる」「リンパ球系血球にのみ分化できる」など系統が限定された多分化能と自己複製能を有する血球。
これまでの造血幹細胞研究のメインアプローチは「移植」。
しかし移植実験の問題点がいくつかある。
- 移植された細胞の中で生着するのは、末梢血内を循環し、ニッチでコロニーを形成し、速やかに増殖できた細胞。→かなり限られた細胞を見ている可能性がある。
- 移植実験によって細胞にかかるストレスは尋常ではない。
→本当に生理的な造血を反映しているか疑問である。
固形組織(他の主要臓器)の幹細胞に比べると造血幹細胞は実験による扱いが難しく、HSCや前駆細胞の数や寿命、系統分化能といった基本的な情報すら十分に解明されているとは言えない(本論文が発表された2014年時点で)。
→筆者らは、体内で本来の場所にある(=in situ)HSCをラべリング・追跡し、細胞起源やその血球産生動態を突き止める方法を本論文で示す。
トランスポゾンによるタグ付技術の開発
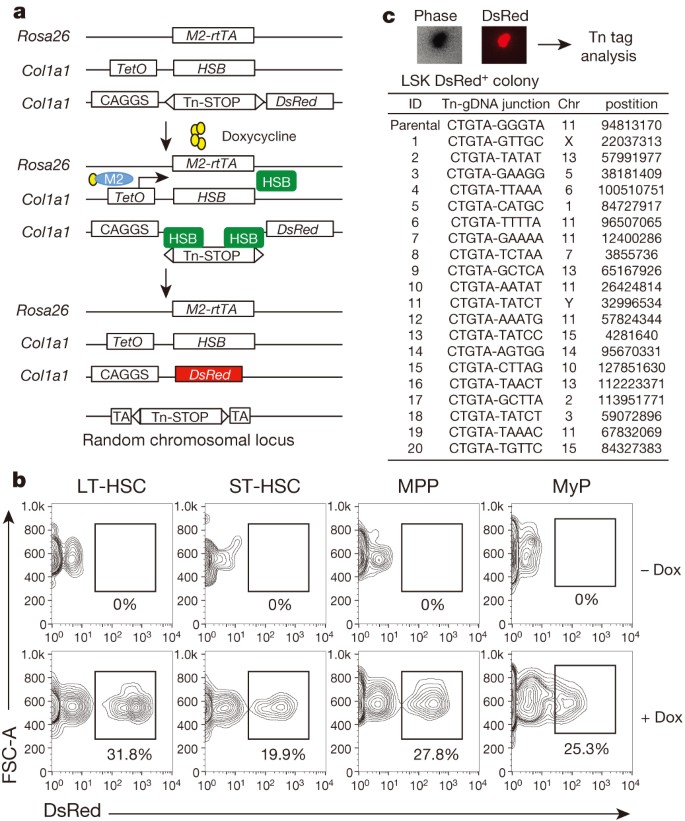
筆者らは、Sleeping beuty transposonを利用し、ドキソルビシンをマウスに入れると、そのタイミングでマウス体内でトランスポゼースが発現し、これによってDsRedが発現するようなシステムを開発した。(下図a)
実際に一定割合DsRed細胞が発現していることを確認。
上図aのCAGGSに相当する部分は、それぞれ異なっている。つまり、DsRed陽性細胞(赤色)の細胞をさまざまな週齢で解析し、その遺伝子配列をシークエンスで読み取れば、細胞起源が分かる。
マウスを使った実験
前述のシステムを遺伝子に備えたマウス(M2/HSB/Tnマウス)を作成。一定期間DOXを投与した後、投与終了後から13週から定期的にマウスの末梢血を採取し、解析。40週の時点でマウスを解剖し骨髄解析を行った。
・顆粒球でDsRed(+)となるのは基本的に(90-98%で)1回のみ(=一時点のみ)。
・2点以上で観察できるとしても基本的に連続したタイムポイントである。
・一方、リンパ球に関しては、Tリンパ球もBリンパ球も、どのポイントでも一定してDsRed(+)となる細胞が多かった。(DsRed(-)の細胞はずっと(-)のまま)
→顆粒球の祖先となる細胞群が存在し、それが安定して大多数の末梢血顆粒球を産生しているわけではないのでは?
顆粒球を安定して長期に産生するためには重複しないクローンの連続的供給による!
クローン運搬と寿命
ある1匹のマウスに一定期間DOXを投与したのち、Off。様々なタイムポイントでDsRed(+)顆粒球細胞を解析。新たな配列のトランスポゾンタグが見つかるたびにナンバリングしていく→ほとんど重複なし(1回DsRed(+)となったら、次のタイムポイントでは基本的に出てこない。)
→1つの細胞集団がずっと長期に顆粒球を産生し続けているわけではない。定期的に入れ替わっている。
これらの実験から、だいたいいくつくらいの数の細胞が顆粒球を産生しているのか数学的に計算→だいたい831±206
※この解析に使っているのはDsRed(+)となっている20-30%程度の細胞のみ。実際はもっと多いはず。
→また観察期間(5-6週ごと)に新しいクローンに入れ替わっている。
長期的に顆粒球を安定して産生するには尋常でない数のクローンが必要!
造血クローンの系統アウトプット
顆粒球とB・Tリンパ球でタグを共有しているものはほとんどなし。
→顆粒球を産生しているクローンは骨髄系統に偏った分化能を示す!
※骨髄球系細胞の1つで顆粒球と同じ起源を有すると考えられる単球は、若齢でも高齢でも経過を通して、顆粒球とのタグ共有率が高い→骨髄球系に偏った分化能を有する顆粒球の起源は少なくとも顆粒球と単球2つの系統への分化が可能。
またリンパ球に関しては、若齢ときにはほぼ顆粒球とのタグの共有はなし、しかし高齢になっていくと共有割合が増えていく。
→リンパ球は、若齢時はリンパ球系統に偏った祖先から産生されているが、週齢が進むと多分化能を有する血球から分化する!

造血クローンの起源
LT-HSCが長期にわたる造血の主要な部分を担っていると考えられてきたが、移植以外の評価はなされてきていなかった。→筆者らはこれを調査。
M2/HSB/TnマウスにDox投与→骨髄をとり出す
→半分移植・半分は顆粒球としてタグ解析
→終了後1年した後に移植→末梢血サンプリングを約1年半継続
もし、ドナーマウスのHSCが定常状態での顆粒球産生を促進するなら、レシピエントマウスにおいてその子孫から同じタグが検出されるはずである。
→ドナー顆粒球タグの内、レシピエントマウスの顆粒球・リンパ球で同じタグが見られたのはわずか5-8%ほど。
移植しなかった半分の顆粒球から検出されたのではないタグをもった血球が、多系統血球産生を行ていた。
次にDox off後40週マウスから様々な骨を取り出し、LT-HSC, MPP, MyPなど様々な分画の骨を解析し、タグ共有があるかチェック。
→顆粒球・単球・Bリンパ球など様々な系統の血球とMPPはタグ共有。しかしLT-HSCはほぼ共有なし!(5%未満)
多系統血球を主に産生しているのはLT-HSCではなく、前駆細胞ではないか?
移植時とは動態が異なっているよう。
Discussion
・成人における多系統血球産生の大部分を担っているのは、HSCではなくMPPではないか?系統制限多能性クローンが数千個あれば事足りる。
・これは非常に高齢のマウスではどうなる?枯渇してしまうのではないか?
・今回の研究によって骨髄悪性腫瘍の起源に関しての知見が深まる。これまではHSC画素の起源だと考えられてきたが、もしかしたらMPPではないか?
・我々の開発したシステムは造血、発達、加齢の研究に今後も役立つであろう。